Material de lectura
1. Repasando
Los secretos del carbono...
Es un elemento químico muy singular cuyos átomos presentan algunas propiedades que revisaremos a continuación.
Como ya has estudiado en tercer año el carbono es el número 6 en la tabla periódica, lo que significa un átomo de carbono tiene 6 protones en su núcleo y 6 electrones en la periferia. Los electrones se encuentran ordenados en niveles, para el caso del carbono la distribución electrónica es la siguiente:
Nivel 1: 2 e-
Nivel 2: 4 e-
Los electrones que se encuentran en el último nivel de energía incompleto se llaman electrones de valencia. El átomo de carbono tiene entonces 4 electrones de valencia (pertenecientes al nivel 2). Si realizamos el diagrama de Lewis(representando cada electrón de valencia con un punto) nos quedaría:

Estos 4 electrones de valencia posibilitan la formación de 4 enlaces covalentes. Por esto se dice que los átomos de carbono son tetravalentes.
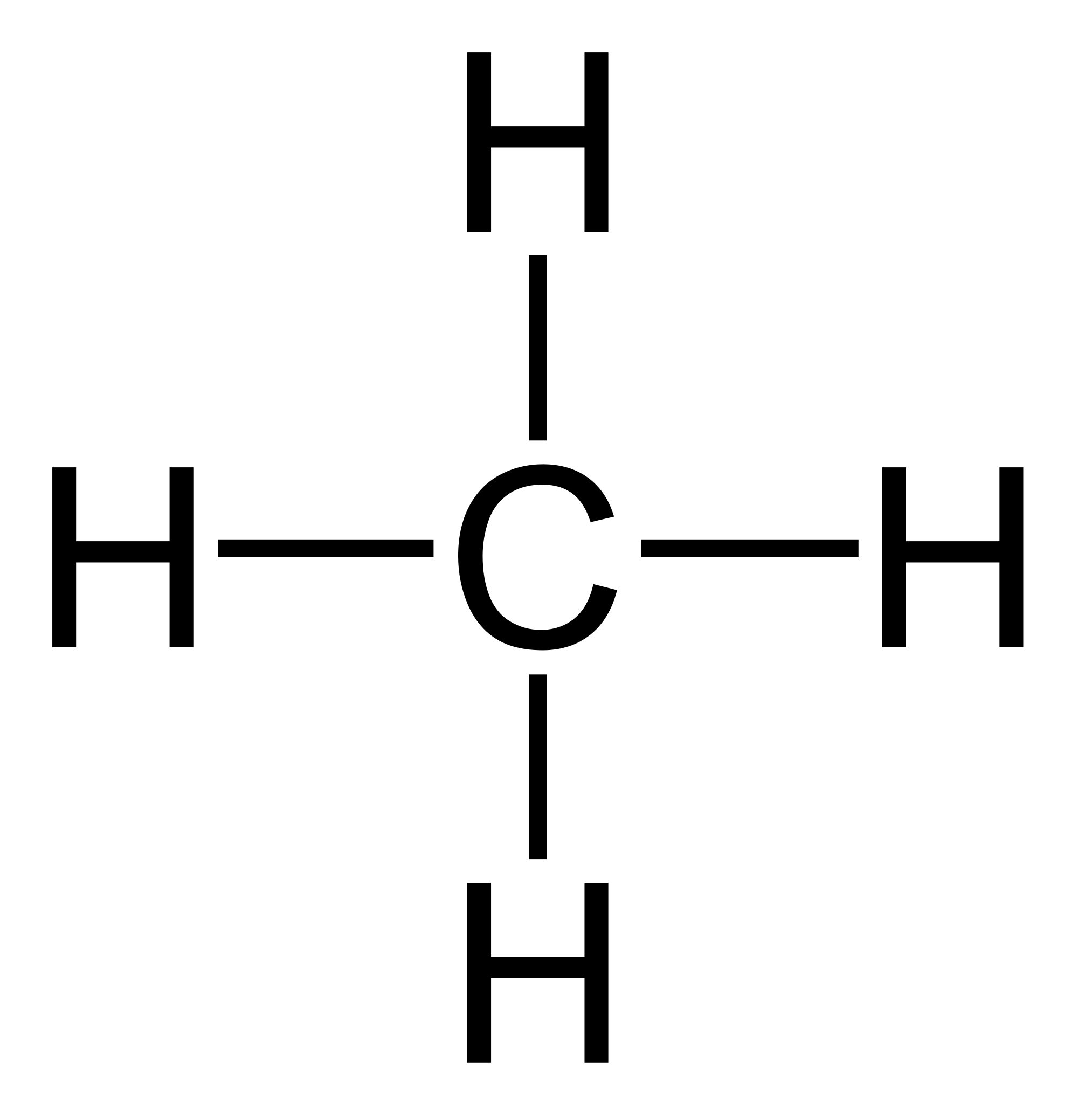
Otra propiedad de los átomos de carbono es laconcatenación, se unen entre sí formando cadenas.
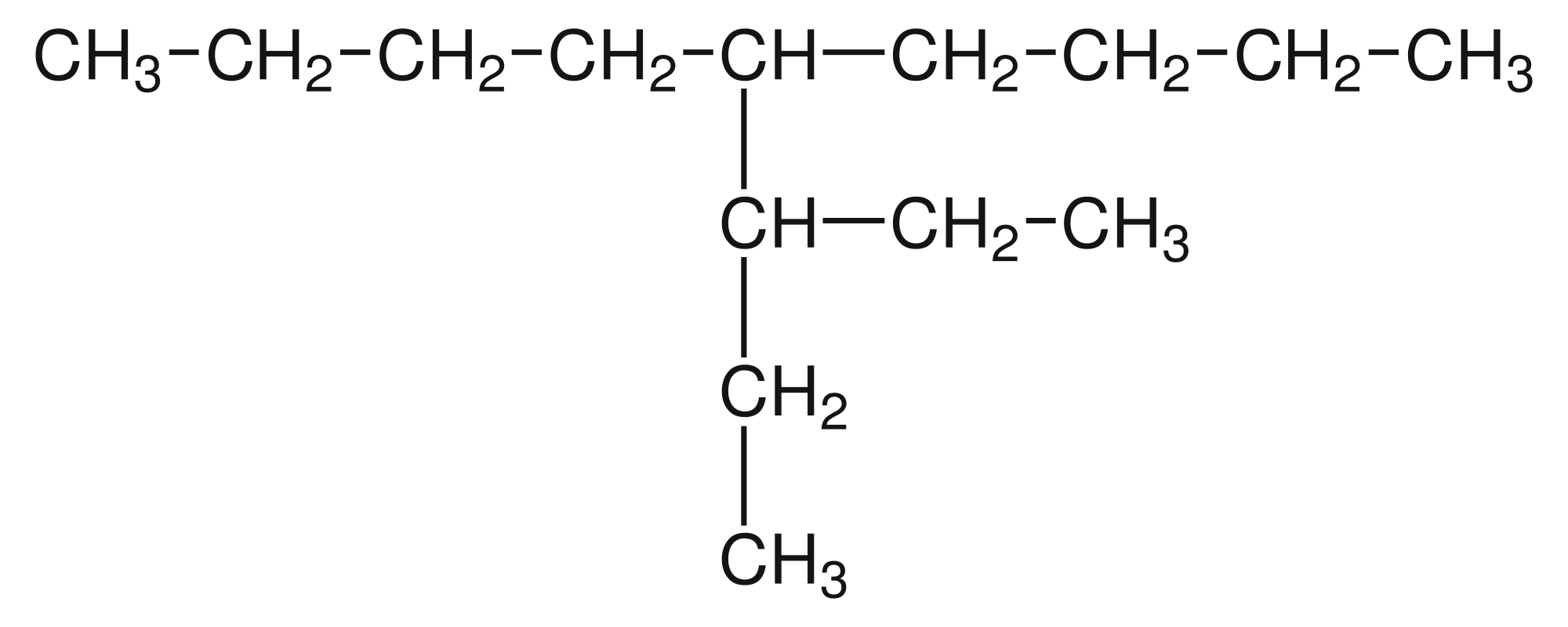
A su vez, las cadenas carbonadas pueden cerrarse formando anillos.
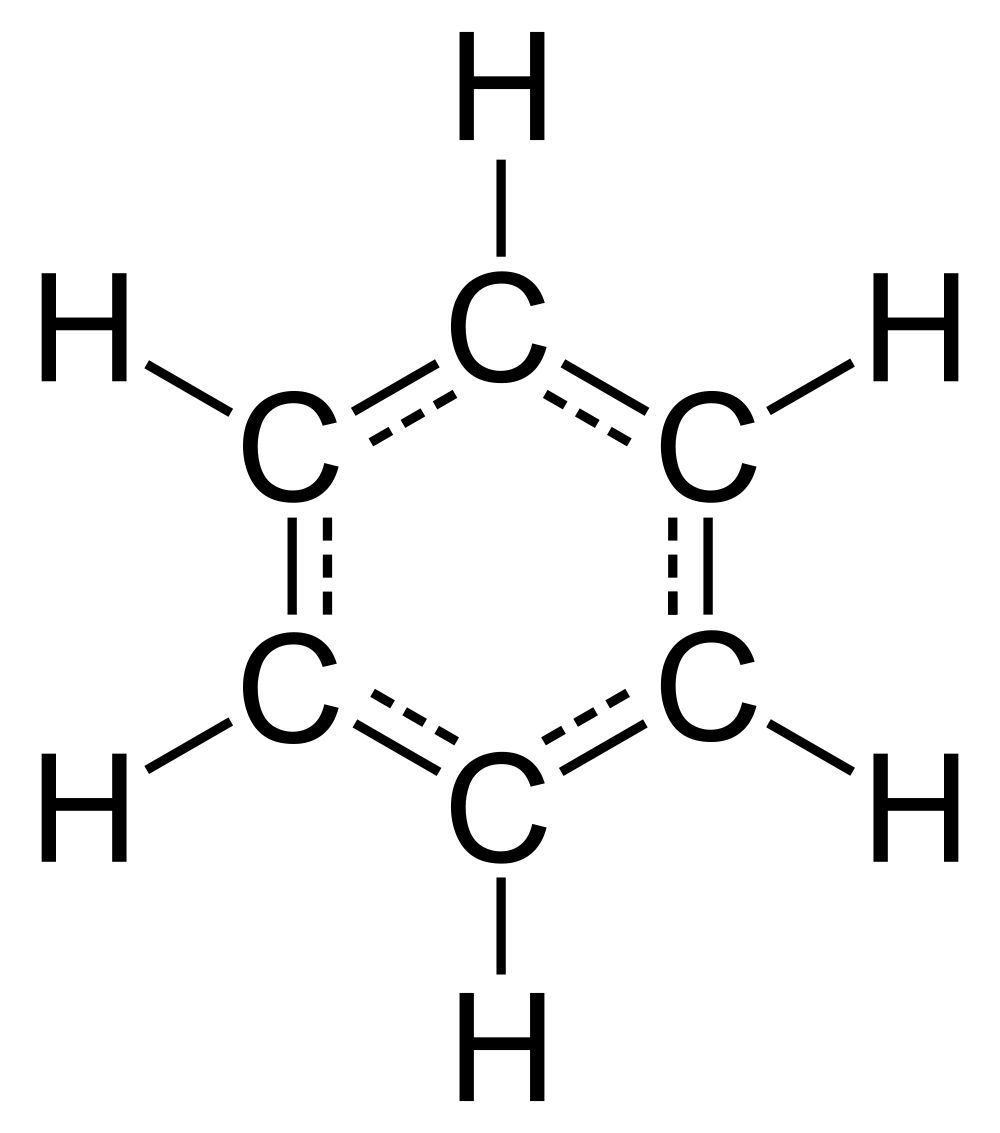
El compuesto anterior (benceno) también se puede representar:
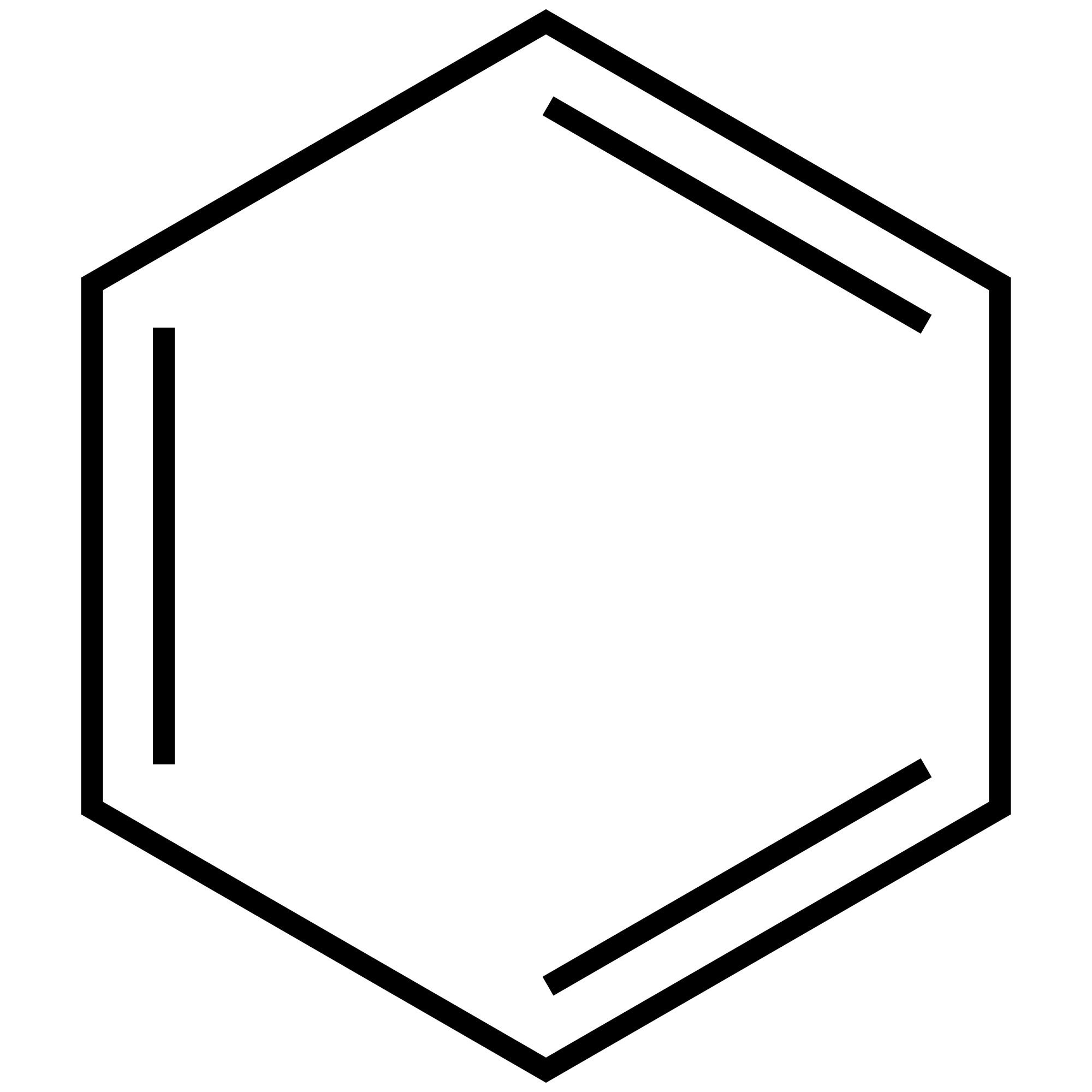
Los átomos de carbono pueden unirse entre sí y con otros átomos de distintos elementos formando:
- enlaces simples (-C-C-, -C-H)
- enlaces múltiples (-C=C-, -C=O, -C≡C-, -C≡N)
Compartiendo uno o más pares de electrones con otro átomo de carbono, de oxígeno, nitrógeno, etc.
Estas propiedades analizadas son la base de los compuestos que estudiaremos en siguientes módulos.