Energía y calor
3. ¿Qué es el calor?
3.4. Variación de temperatura, masa y calor específico
A partir de datos experimentales se puede concluir que el calor es directamente proporcional a la variación de temperatura.
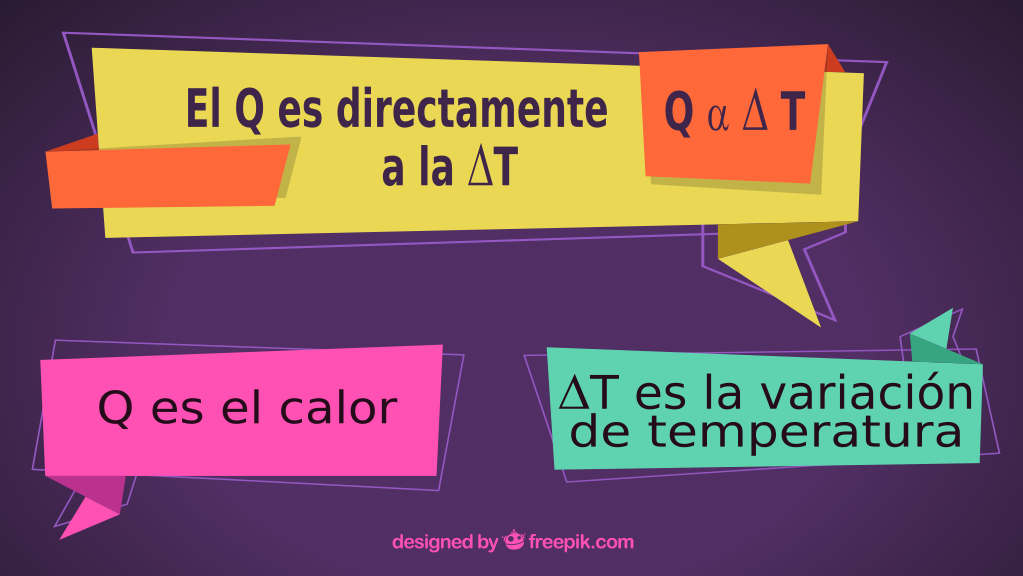
La variación de temperatura, se calcula restando la temperatura final y la temperatura inicial (Δt = tfinal - tinicial).
A partir de datos experimentales se puede concluir que el calor es directamente proporcional a la masa.

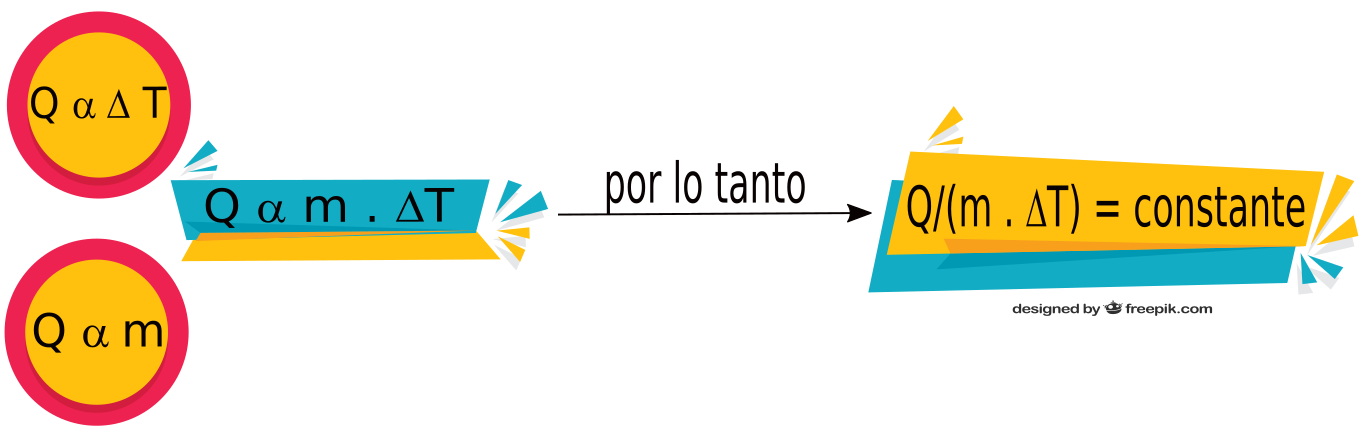
Por lo tanto sabemos que: Q α (es directamente proporcional) Δt y también es directamente proporcional a la masa.
Podemos decir entonces que Q α m. Δt (el calor es directamente proporcional al producto entre la masa y la variación de temperatura).
Si calculamos el cociente entre el calor y el producto de la masa y la variación de temperatura (m . ΔT) obtenemos un valor constante:
Q / m . ΔT = constante
El valor constante que se obtiene al hacer el cociente Q/(m . ΔT ), es diferente para cada sustancia o material, y es una propiedad intensiva característica denominada Calor Específico. La notación que se utiliza para denominar al Calor Específico es Ce.

El calor específico de una sustancia o material, cuya notación es "Ce", es la cantidad de energía que hay que suministrar a 1 gramo de la misma para que su temperatura aumente 1 °C.
Las unidades más utilizadas del calor específico son: J/g°C o cal/g°C.