¿Qué factores y variables modifican la rapidez de una reacción química?
1. Introducción
![]()
Cualquier reacción química se produce mediante choques o colisiones entre las partículas de reactivo. Para que se forme una nueva sustancia, los enlaces que mantienen unidas a las partículas que reaccionan primero deben romperse, para posteriormente originar nuevos enlaces, formándose nuevos compuestos como productos de reacción.
Así, por ejemplo, si tenemos la reacción:
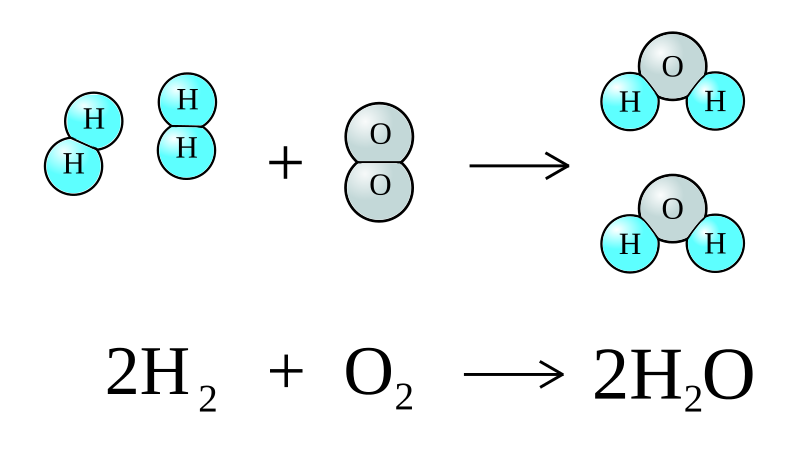
2 H2 (g) + O2 (g) → 2 H2O (g)
Los enlaces de las moléculas de H2 y de O2 deben primero romperse, para que los átomos de
hidrógeno puedan combinarse con los de oxígeno. Pero para ello es necesario que los choques
entre moléculas se produzcan con un mínimo de energía y una buena
orientación. A continuación profundizaremos en estos dos aspectos.