Clasificación, monosacáridos, disacáridos y polisacáridos
| Sitio: | Aulas | Uruguay Educa |
| Curso: | Química - 3º B.D. |
| Libro: | Clasificación, monosacáridos, disacáridos y polisacáridos |
| Imprimido por: | Invitado |
| Día: | lunes, 7 de abril de 2025, 09:06 |
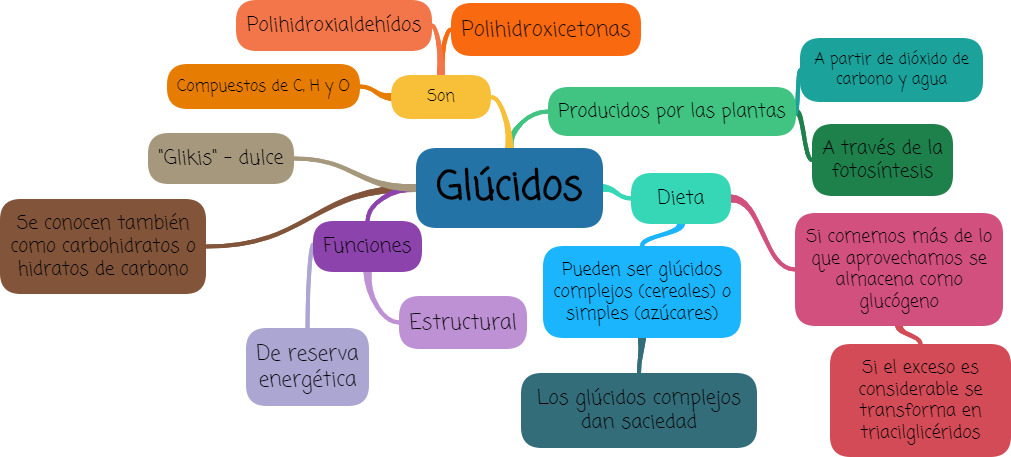
1. Glúcidos
Griego: “glikis”: dulce. Los glúcidos son una de las tres principales clases de nutrientes. Representan una de las más importantes fuentes de energía en la dieta.
Contienen carbono, hidrógeno y oxígeno. Son POLIHIDROXIALDEHÍDOS o POLIHIDROXICETONAS.
Cumplen funciones de reserva y estructural.Son producidos por plantas a partir de dióxido de carbono, agua y energía a través del proceso llamado fotosíntesis. Los animales y el hombre son incapaces de sintetizar glúcidos, a diferencia de las plantas.
La mayor parte de los glúcidos que consumimos deben ser glúcidos complejos como los que se encuentran en los cereales, no los azúcares simples ya que no dan saciedad.
Cuando comemos más de lo que podemos aprovechar, se almacenan pequeñas cantidades de glúcidos en el hígado y en los tejidos musculares en forma de glucógeno. Si el exceso es considerable, los glúcidos se convierten en grasa y se almacenan como triglicéridos.
1.1. Clasificación
- No
hidrolizables: son los glúcidos más sencillos llamados monosacáridos, monosas u osas.
- Hidrolizables:
Mediante hidrólisis se obtienen 2 o más monosacáridos, nombrándose:
|
Nombre |
Monosacáridos obtenidos por hidrólisis |
|
Disacáridos |
2 |
|
Trisacáridos |
3 |
|
Oligosacáridos |
4 a 10 |
|
Polisacáridos |
Más de 10 |
HIDRÓLISIS: reacción donde intervienen moléculas de agua provocando la rotura de enlaces y como consecuencia la descomposición.
1.2. Grupos funcionales presentes
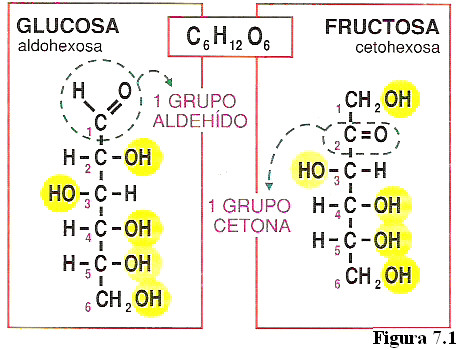
En amarillo se representan los grupos hidroxilo (función característica de los alcoholes).
Pueden tener un grupo aldehído (carbonilo): polihidroxialdehídos.
O un grupo cetona (carbonilo): polihidroxicetonas.
2. Monosacáridos
Son las unidades fundamentales de los glúcidos.
No son hidrolizables.
Consisten en una sola unidad de polihidroxialdehído o polihidroxicetona.
La mayoría tienen sabor dulce.
Si el grupo carbonilo se halla en un extremo de la cadena carbonada, el monosacárido recibe el nombre de ALDOSA; si el grupo se encuentra en cualquier otra posición se denomina CETOSA.
Algunos ejemplos: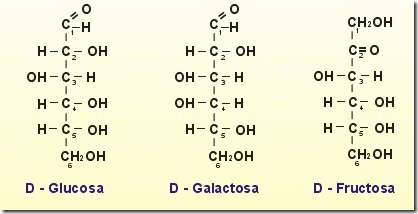
2.1. Glucosa
Conformaciones de la glucosa cíclica:
Los monosacáridos con 5 o más átomos de C en su cadena suelen encontrarse en solución acuosa en forma de estructuras cíclicas (en anillo), en las que el grupo carbonilo ha formado un enlace covalente con el oxígeno de un grupo hidroxilo perteneciente a la misma cadena.
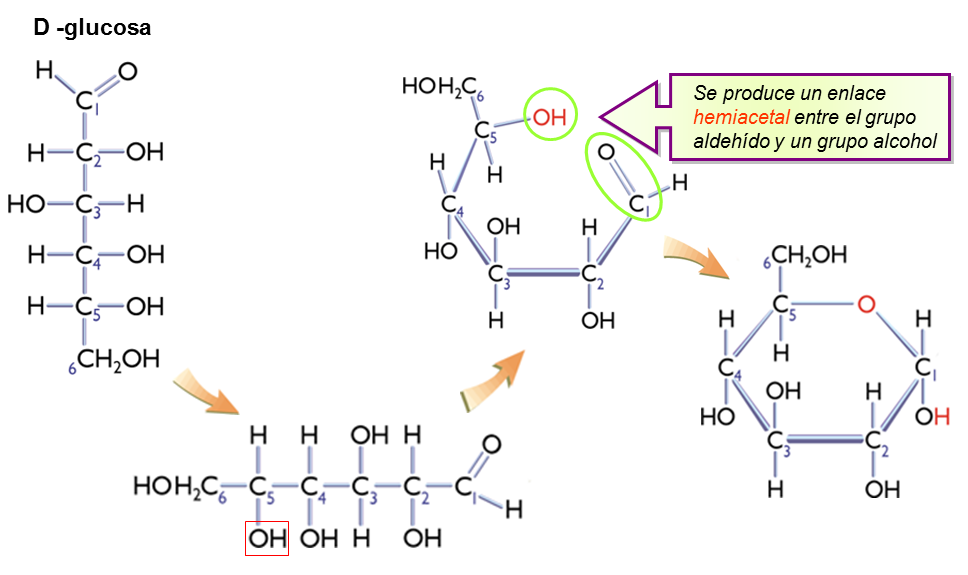
- α (el grupo hidroxilo del primer carbono, en violeta en la segunda imagen, se encuentra hacia "abajo") y
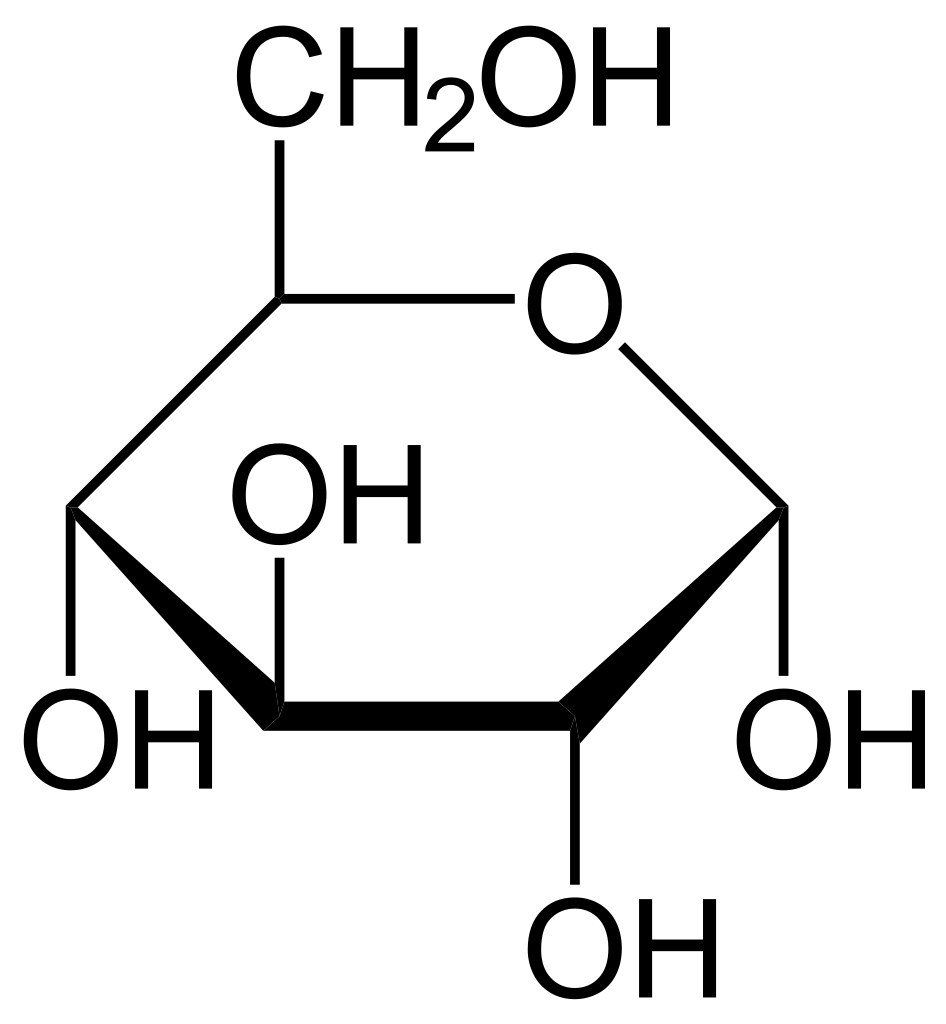
α-D-glucopiranosa o α-glucosa
- β (el grupo hidroxilo del primer carbono se encuentra hacia "arriba").
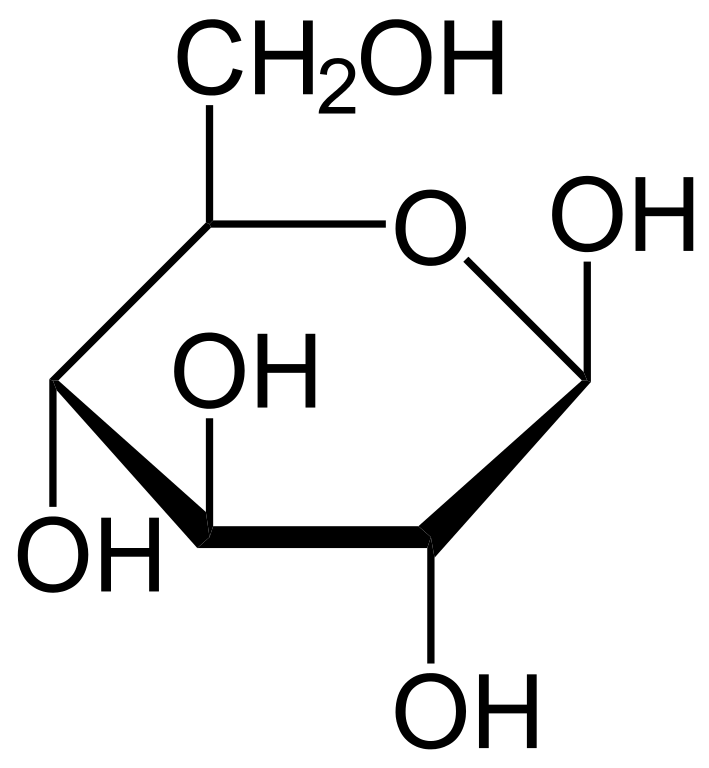
β-D-glucopiranosa o β-glucosa
FÓRMULA DE PROYECCIÓN HAWORTH:
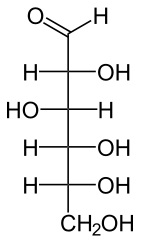
FÓRMULA DE PROYECCIÓN FISCHER:
También se puede representar a la glucosa de cadena abierta de la siguiente manera (más simplificada) denominada fórmula de Fischer.
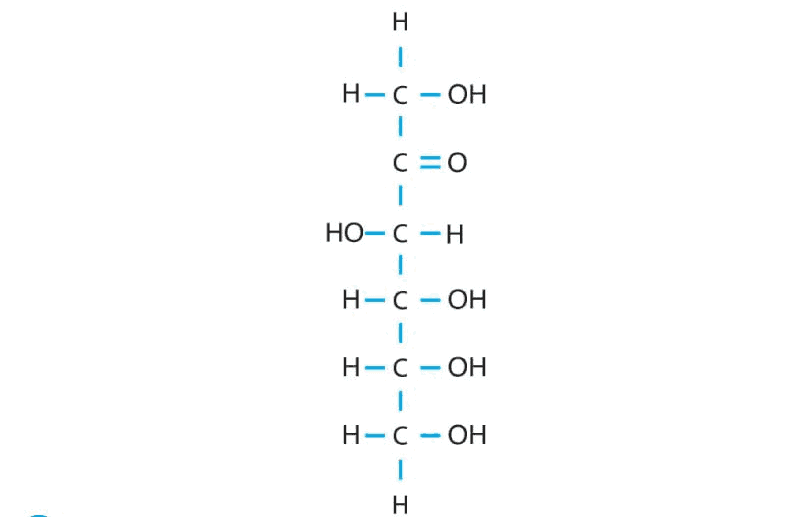
2.2. Fructosa
Se encuentra principalmente en las frutas.
Es una cetosa de 6 átomos de Carbono.
Conformaciones de la fructosa cíclica:
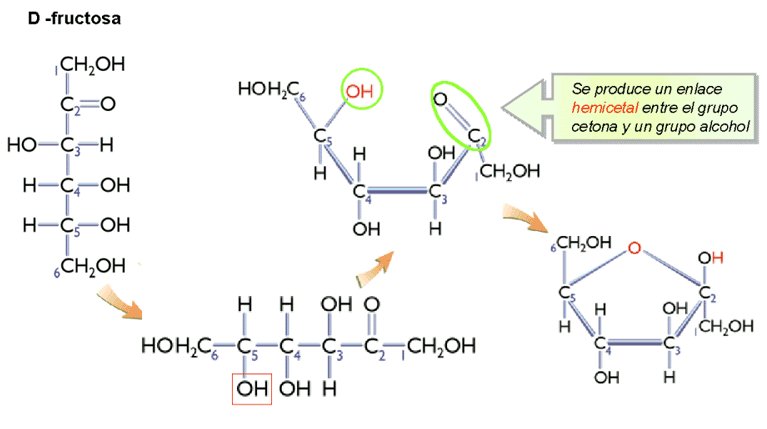
FÓRMULA DE PROYECCIÓN HAWORTH:
Las aldosas presentan también formas cíclicas con anillos de 5 átomos que por su similitud con el compuesto cíclico furano, formado por un anillo de 5 átomos, se denominan furanosas.
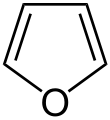
Estructura del furano.
Las cetohexosas, como la fructosa, se encuentran también en sus formas anoméricas α y β. En estos compuestos el grupo hidroxilo en C-5 reacciona con el grupo cetona en C-2, formando un anillo de furanosa que contiene un enlace de tipo hemicetal.
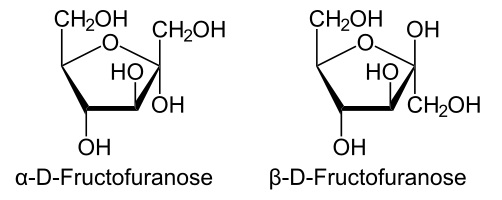
α-fructosa β-fructosa
FÓRMULA DE PROYECCIÓN FISCHER:
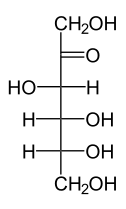
3. Disacáridos
Consta de 2 monosacáridos unidos covalentemente por un enlace glicosídico o glucosídico (si los monómeros son de glucosa exclusivamente).
Un grupo hidroxilo del carbono anomérico del primer monosacárido reacciona con un hidroxilo unido a un carbono (anomérico o no) del segundo monosacárido. El proceso es una condensación en donde se libera una molécula de agua.
Si la reacción de los OH provienen de los dos carbonos anoméricos, el disacárido será dicarbonílico, los dos grupos -OH se ven involucrados en el enlace, y no tendrá poder reductor ya que este reside en el grupo -OH. Sin embargo, si en el enlace participan los OH de un carbono anomérico y de otro carbono no anomérico, el disacárido será monocarbonílico y tendrá poder reductor (ya que queda un grupo OH libre en el otro carbono anomérico). Este hecho se puede comprobar experimentalmente mediante la reacción con el reactivo de Fehling o con el reactivo de Tollens como se analizará más adelante.
Son hidrolizables por acción de ácidos pero son resistentes a la hidrólisis básica. Al formarse el enlace se forma una molécula de agua.
EJEMPLOS:
- MALTOSA
- LACTOSA
- SACAROSA
- CELOBIOSA
Por convención, el nombre describe el compuesto escrito con su extremo no reductor a la izquierda mientras que el nombre "se construye" siguiendo el siguiente orden:
- Se da la configuración (α o β) del átomo de carbono anomérico que une la primera unidad del monosacárido (izquierda) con la segunda.
- Se añade el enantiómero (D o L) de cada uno.
- Se indica la estructura del anillo de cada monómero (furano o pirano).
- Se añade la terminación -osil al primer monosacárido.
- Los dos átomos de carbono unidos por el enlace glicosídico se indican entre paréntesis, con una flecha que conecta los dos números; por ejemplo, (1→4) indica que el C-1 del primer residuo de azúcar se une al C-4 del segundo.
- Se escribe el segundo monosacárido siguiendo las reglas anteriores. Si el enlace es dicarbonílico termina en -ósido; si el enlace es monocarbonílico termina en -osa.
3.1. Maltosa
- MALTOSA: Azúcar de malta. Se usa en alimentos para niños y en la leche malteada. Es fundamental en la elaboración de la cerveza.
Está formado por dos residuos de α-D-glucosa con enlace α (1-4). 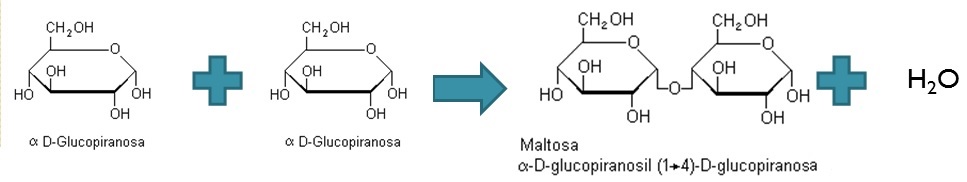
3.2. Lactosa
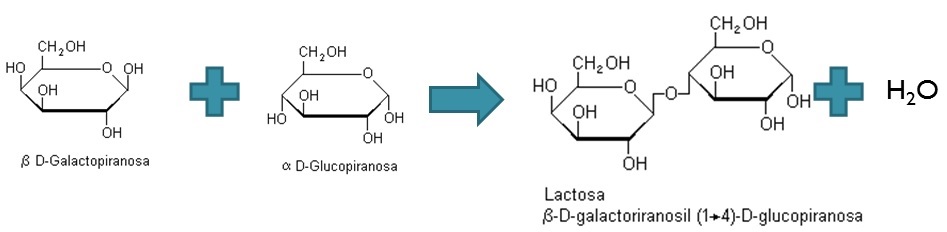
- LACTOSA: Azúcar de la leche. Se encuentra presente en la leche de los mamíferos. En la leche humana tiene una concentración de 5 a 8 g por cada 100 g de leche, y en la de vaca de 4 a 6 g. Comercialmente se obtiene como subproducto al fabricar el queso.
Da lugar a β-D-galactosa y α -D-glucosa por hidrólisis.
3.3. Sacarosa
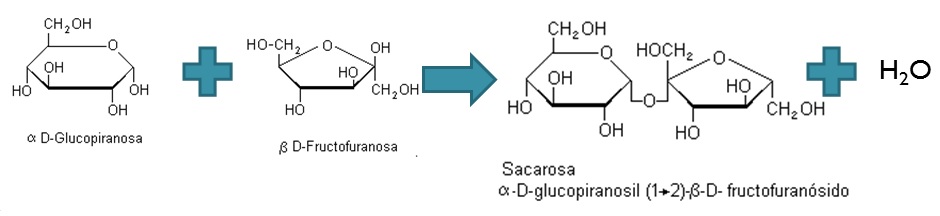
- SACAROSA: Azúcar de mesa. Se obtiene de la caña de azúcar y de la remolacha azucarera.
Da lugar a α-D-glucosa y β-D-fructosa por hidrólisis.
3.4. Celobiosa
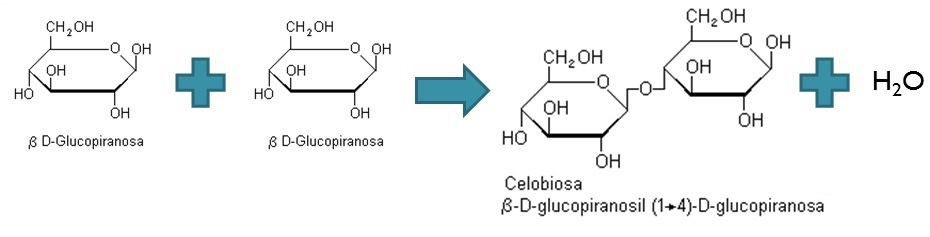
- CELOBIOSA: Se obtiene de la hidrólisis de la celulosa.
Da lugar a dos unidades de β-D-glucosa por hidrólisis.
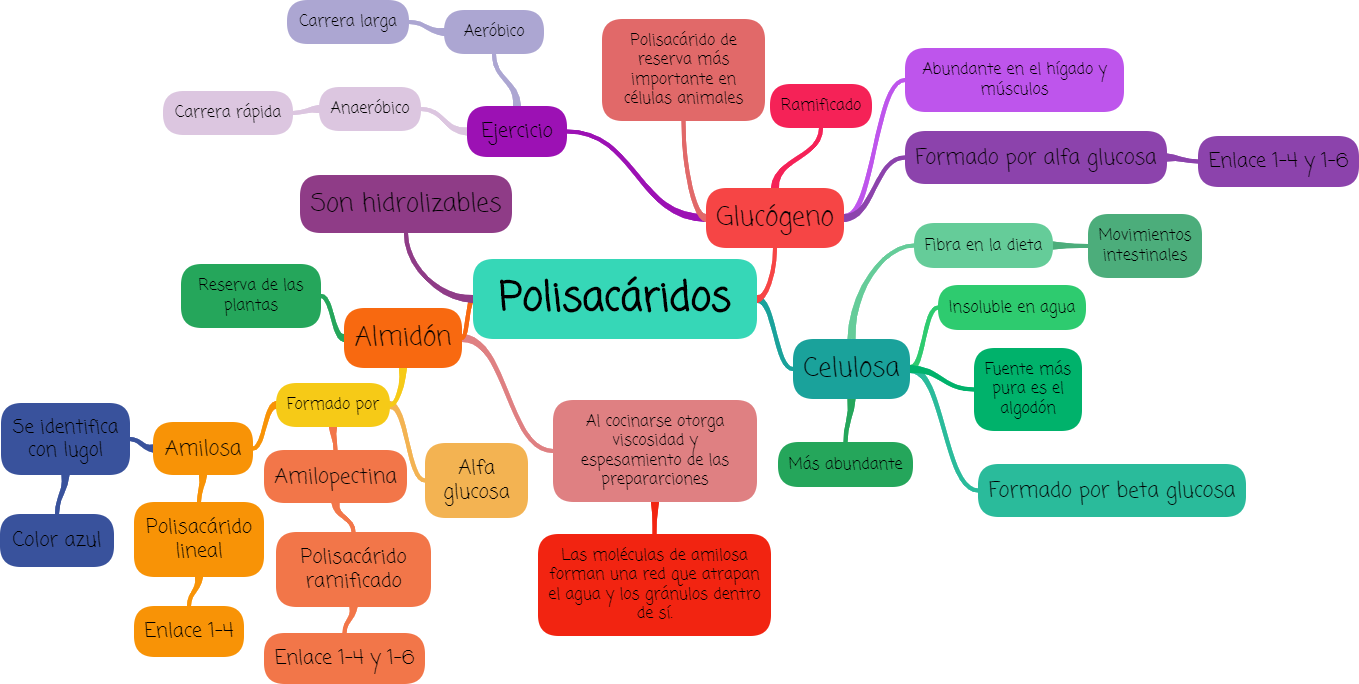
4. Polisacáridos
Muchas unidades de monosacáridos unidos covalentemente por enlace glicosídico.
Son hidrolizables en glúcidos más sencillos.
La mayoría de los glúcidos naturales se encuentran en forma de polisacáridos.
En una dieta equilibrada se necesita ingerir un 55 % de glúcidos (40 % polisacáridos – ya que dan más saciedad- y un 15 % de monosacáridos/disacáridos)
EJEMPLOS:
- ALMIDÓN
- CELULOSA
- GLUCÓGENO
4.1. Almidón
- ALMIDÓN: Es la forma más importante de reserva de glúcidos de las plantas. Contiene dos tipos de polímeros de glucosa, amilosa y amilopectina. Casi todos los almidones son una mezcla de un polisacárido lineal, la AMILOSA (soluble), y un polisacárido ramificado la AMILOPECTINA (insoluble). Presenta enlace α (1-4).
4.2. ¿Cómo identificar almidón en muestras?
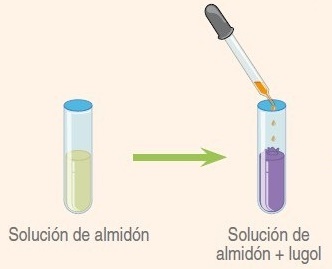
Coloración del almidón con lugol:
En términos generales, los almidones contienen aproximadamente 17-27 % de amilosa, y el resto de amilopectina.
El diyodo (en el reactivo de lugol se encuentra como I3-) reacciona con la amilosa y genera un fuerte color azul característico debido al complejo que se establece entre una molécula de éste con cada 7-8 glucosas; para desarrollar adecuadamente la coloración se requiere un mínimo de 40 residuos de monosacárido, las cadenas muy cortas de amilosa, en lugar de azul producen un color rojo.
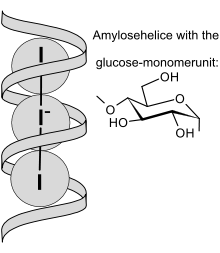
Aparentemente el complejo amilosa-yodo se establece por la inclusión del I3- en la hélice.
Por otra parte, la amilopectina sólo forma complejos con una pequeña cantidad de I3- y desarrolla una coloración roja.
Observa el siguiente video:
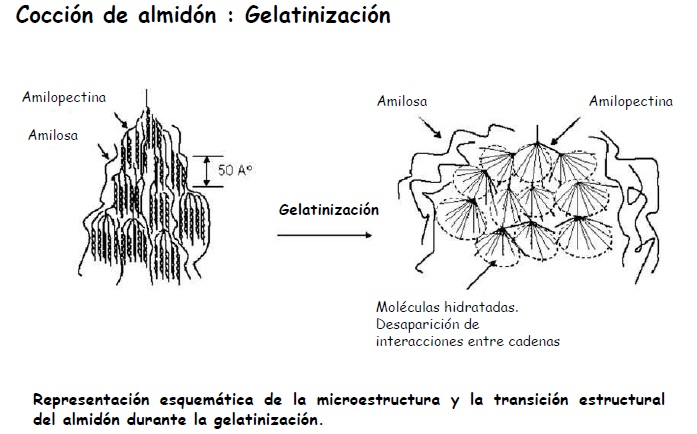
4.3. ¿Qué sucede al cocinar el almidón?
¿Qué ocurre al cocinar el almidón?Al aumentar la temperatura del sistema almidón y agua, los gránulos de almidón modifican su estructura y gracias a la asociación de la amilosa y la amilopectina con el agua, transforman su consistencia: se habrán "disuelto" y se perderá el sabor a crudo. Cuando los gránulos pierden toda su estructura cristalina habrán gelatinizado.
El término gelatinización indica la completa hidratación del almidón, no la formación de un gel.
Analicemos lo que ocurre al preparar una salsa o crema en base a almidón:
- El primero paso es dispersar el almidón en agua a temperatura ambiente con el objetivo que los gránulos se separen lo más posible antes de comenzar a calentar la preparación.
- Cuando la temperatura se eleva alrededor de los 57 ºC, los gránulos de almidón comienzan a abrirse por las partes más débilmente asociadas. Esta apertura permite la entrada de agua que se asocia a las moléculas de amilosa y amilopectina y hace que los gránulos se vayan hinchando. A su vez, las moléculas de amilosa salen al medio acuoso y se asocian con el agua que está por fuera del gránulo.
- El aumento de la temperatura aumenta el movimiento de las moléculas y, entonces, se vence la atracción que las moléculas tienen entre sí por lo que al encontrarse con las moléculas de agua (que están en el medio y en gran cantidad) las moléculas de amilosa se asociarán con las de agua. Esta asociación impide que el líquido se desplace fácilmente. Así se genera el espesamiento, junto a la inmovilización de agua dentro de los gránulos asociada a la amilopectina que, por su gran tamaño no puede salir del gránulo.
Pensemos en la siguiente analogía: si agregamos bombitas llenas de agua a un balde con agua, cuántas más agregamos, más difícil será mover el agua que hay entre ellas. Si por alguna razón se rompen el agua podrá moverse libremente otra vez. En el caso de la salsa o crema, si agitamos o calentamos demasiado la preparación se hará más fluida y no podremos revertir este cambio, por eso no conviene sobrecalentar la crema o salsa cuando ya está pronta.
La viscosidad y textura de la preparación dependen de:
- La proporción amilosa-amilopectina: la textura que brinda la amilopectina se parece a un chicle brilloso, es suave, transparente y no fluye con facilidad. La amilosa, en cambio, da un aspecto opaco, su textura es áspera y fluye de manera diferente.
- El tamaño de los gránulos: los almidones cuyos gránulos sean menores darán un mayor espesamiento. Volviendo a la analogía: si las bombitas son más pequeñas, el movimiento será más difícil.
- Tamaño de las moléculas de amilosa: cuanto más largas sean las moléculas, más habilidad tendrán para impedir el movimiento del agua y, por lo tanto, espesarán más la preparación.
- Procedimiento usado: uso de batidor, cuchara, calentamiento, etc.

¿Por qué se sugiere agregar el almidón en el líquido que se quiere espesar revolviendo con un batidor?
Así provocamos la dispersión de todas las partículas que contienen los gránulos de almidón. Esto permitirá que no formen grumos cuando comiencen a asociarse con el agua, ya que si los gránulos de almidón están juntos forman un gel que impide la entrada de más agua y se generan los indeseables grumos.
_______________________________________
Para pensar... Puré pisado versus puré procesado (mixer)
¿Qué diferencias observas entre ambos tipos de puré?
¿Cómo lo explicas?
4.4. ¿Qué sucede cuando la preparación espesada con almidón se "enfría"?
ENFRIAMIENTO:
Si enfriamos una preparación espesada con almidón, esta aumentará su viscosidad. Algunas de ellas, además, conservarán la forma del molde al ser desmoldadas, es decir que habrán formado un gel. Para que esto sea posible, el almidón en cuestión debe poseer una proporción suficiente de amilosa; por ello las salsas espesadas con almidón procedente de mandioca (que no tiene casi nada de amilosa) no conservan la forma. Para obtener un gel firme será necesario que los gránulos de almidón se hayan hinchado y que haya amilosa suficiente tanto en cantidad como en calidad. Las moléculas de amilosa no deben ser afectadas por ácidos, enzimas, calor, etc. y además deberán provenir de alimentos cuyas cadenas sean lo suficientemente largas para poder formar una red.
La adición de enzimas (como las alfa amilasas) cortan el almidón y disminuyen el tamaño de las amilosas, en consecuencia la preparación espesa menos. ¿En qué alimentos encontramos estas enzimas? Están presentes en la harina de trigo, pero como se trata de proteínas, si primero se hace un roux, se inactivan debido al calentamiento. También se encuentran en la yema de huevo y por lo tanto, si se agrega una yema a una preparación se la debe calentar (lo suficiente para inactivar las enzimas pero no tanto para coagular las proteínas presentes en las yemas) para que la mezcla mantenga viscosidad.
¿Por qué se forma la red? Luego de haber calentado el almidón y de que este haya perdido su forma cristalina, se asociará con el agua. Mientras la temperatura se mantenga elevada, las moléculas tendrán alta energía cinética, es decir, se estarán moviendo. Cuando la temperatura comience a bajar, el movimiento disminuirá, con lo cual las atracciones entre moléculas de amilosa serán más fuertes que su energía para moverse; de esta manera, se irán acercando y formando una red entre sí que atrapará al agua y los gránulos de almidón hinchados. Si hay poca amilosa o las cadenas son cortas, no alcanzarán para formar la red deseada o bien esta será muy frágil.
El paso del tiempo...
Al pasar el tiempo la preparación va cambiando su textura. Las moléculas de amilosa continúan atrayéndose, se acercan más, y por lo tanto, se libera agua de la red. Este proceso se llama "sinéresis", y lo podemos observar a simple vista cuando vemos gotitas de agua en nuestra salsa o crema.

4.5. Celulosa
- CELULOSA: Es el polisacárido más abundante, y la fuente de celulosa más pura es el algodón. Da lugar a β-D-glucosa por hidrólisis completa y su hidrólisis parcial da celobiosa. Es insoluble en agua. Los seres humanos no pueden digerirla (fibra en la dieta).

4.6. Glucógeno
- GLUCÓGENO: Es el polisacárido de reserva más importante en las células animales. Al igual que la amilopectina, el glucógeno es un polímero con subunidades de glucosa unidas por enlaces α (1-4) y ramificaciones del tipo α (1-6), pero el glucógeno está más ramificado y es más compacto que el almidón. El glucógeno es especialmente abundante en el hígado.
Ejercicio aeróbico: Los músculos almacenan una provisión amplia de energía en forma de glucógeno. Cuando se inicia la contracción muscular, las células musculares convierten el glucógeno, por medio de una serie de etapas, en ácido pirúvico. Luego si se disponde de suficiente dioxígeno y otros factores, el ácido pirúvico se oxida mediante una serie de pasos, a dióxido de carbono y agua. Las contracciones musculares que se producen en estas circunstancias, es decir, en presencia de dioxígeno, constituyen el ejercicio aeróbico.
(C6H12O6)n → 2n CH3COCOOH
glucógeno → ácido pirúvico
2 CH3COCOOH + 5 O2 → 6 CO2 + 4 H2O
Ejercicio anaeróbico: Si no se cuenta con suficiente dioxígeno, el ácido pirúvico se reduce para formar ácido láctico. Si el ejercicio persiste, se acumula un exceso de ácido láctico en las células musculares. El atleta sufre fatiga muscular severa. Una vez que termina el ejercicio, la demanda de dioxígeno de las células disminuye y se cuenta con más dioxígeno para oxidar el ácido láctico y convertirlo otra vez en ácido pirúvico.

Un atleta que se entrena para una carrera rápida realiza mucho trabajo anaeróbico, pero uno que planea correr una carrera larga realiza principalmente trabajo aeróbico. Las carreras cortas y el levantamiento de pesas son en gran medida actividades anaeróbicas; una carrera de maratón es principalmente aeróbica. Durante una maratón, los atletas deben establecer un paso al que puedan correr varias horas. Sus células musculares dependen de la conversión aeróbica, lenta y constante de glúcidos en energía. Durante las actividades anaeróbicas, en cambio, las células musculares casi no consumen dioxígeno, sino que utilizan la energía rápida que proporciona el metabolismo anaeróbico.
Una vez agotadas las reservas de glucógeno, las células musculares pueden cambiar al metabolismo de grasas. Las grasa son la principal fuente de energía para la actividad sostenida de intensidad baja o moderada, como la última parte de una maratón.
5. Créditos
Autoría de los materiales utilizados: Profesora Anarella Gatto.
Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Bibliografía consultada:
- Lehninger y otros. (2005). Principios de Bioquímica. Omega.
- Badui, S. (2006). Química de los alimentos. (Cuarta edición). México: Pearson.
- Alegría, Mónica y otros. (1999). Química II. Argentina: Santillana
- Koppmann, M (2011). Manual de Gastronomía Molecular. (2da Edición). Buenos Aires, Argentina: Siglo Veintiuno.
- Saravia, G., Segurola, B., Franco, M. y Nassi, M. (2012). Todo se transforma. Química- 4º Año (1º BD). Montevideo, Uruguay: Contexto.
- Hill, J. y Kolb, D. (1999). Química para el nuevo milenio (8va edición). México: Pearson Prentice Hall.
- Teijón Rivera, J. y Garrido Pertierra, A. (2006). Fundamentos de bioquímica estructural (2da edición). Madrid, España: Tebar.
Videos, páginas y/o simuladores utilizados:
- Ruben Sebastian. (2015, octubre 13). Glúcidos: Introducción. [Archivo de video]. Recuperado de: https://youtu.be/dCiHPZIzmlo
- Ruben Sebastian. (2015, octubre 25). Proyección de Haworth y ciclación de monosacáridos. [Archivo de video]. Recuperado de: https://youtu.be/1rceTpz4fEo
- Ruben Sebastian. (2015, noviembre 11). Maltosa: como se forma y estructura (disacáridos). [Archivo de video]. Recuperado de: https://youtu.be/1nchlVpr0WA
- Ruben Sebastian. (2015, noviembre 10). Lactosa: como se forma y estructura (disacáridos). [Archivo de video]. Recuperado de: https://youtu.be/sd1DgkmmMSs
- Ruben Sebastian. (2015, noviembre 12). Sacarosa: como se forma y estructura (disacáridos). [Archivo de video]. Recuperado de: https://youtu.be/8GuKnNg2lwY
- Ruben Sebastian. (2015, noviembre 8). Celobiosa: como se forma y estructura (disacáridos). [Archivo de video]. Recuperado de: https://youtu.be/ir7Xks_GeTc
- Ruben Sebastian. (2016, enero 26). Almidón: amilosa y amilopectina / Biología. [Archivo de video]. Recuperado de: https://youtu.be/kMjNM0rJXVw
- Ruben Sebastian. (2016, enero 27). Glucógeno o glicógeno / Biología. [Archivo de video]. Recuperado de: https://youtu.be/DNip2Poh_VQ
- Ruben Sebastian. (2016, enero 28). Celulosa / Biología. [Archivo de video]. Recuperado de: https://youtu.be/2IXLel_bq-o
Videotutoriales Informática Educativa . (2016, diciembre 13). Reacción de Lugol. [Archivo de video]. Recuperado de: https://youtu.be/NIxsxbphsKE
Las imágenes utilizadas fueron tomadas de:
- Grupos funcionales en glucosa y fructosa. https://i0.wp.com/cuadroscomparativos.com/wp-content/uploads/2016/06/78e1a5ce-1e30-4e1a-92f8-aee5504c62daimage7.jpeg?resize=457%2C350
- Fórmula de glucosa, galactosa y fructosa. http://biologia.laguia2000.com/wp-content/uploads/2010/01/hexosas_thumb.gif
- Ciclación de la glucosa. https://lidiaconlaquimica.files.wordpress.com/2015/06/ciclacion-glucosa-aldosas.png?w=561&h=333
- Ciclación de la glucosa 2. https://sites.google.com/site/labiotecaedu/_/rsrc/1472868372501/biomoleculas-los-glucidos/gl%C3%BAcidos11.JPG
- Anómero alfa de la glucosa. https://upload.wikimedia.org/wikipedia/commons/thumb/c/c6/Alpha-D-Glucopyranose.svg/245px-Alpha-D-Glucopyranose.svg.png
- Anómero beta de la glucosa. https://upload.wikimedia.org/wikipedia/commons/8/82/Beta-D-Glucopyranose.svg
- Fórmula de Fischer de la ribosa. https://coloide.files.wordpress.com/2011/03/1-ribosa.jpg
- Fórmula desarrollada de la fructosa. http://www.manualmoderno.com/apoyos_electronicos/9786074482911/imagenes/cap_13/4.jpg
- http://fisicayquimica4.wikispaces.com/file/view/glu11.jpg/427093888/635x358/glu11.jpg
- Anómeros alfa y beta de la fructosa. https://upload.wikimedia.org/wikipedia/commons/thumb/6/6f/D-Fructose_Haworth.svg/505px-D-Fructose_Haworth.svg.png
- Fórmula de Fischer de la fructosa. https://upload.wikimedia.org/wikipedia/commons/thumb/e/e5/D-Fructose.svg/1200px-D-Fructose.svg.png
- Fórmula del furano. https://es.wikipedia.org/wiki/Archivo:Furan.svg
- Fórmula del pirano. https://es.m.wikipedia.org/wiki/Archivo:2H-Pyran.svg
- Ciclación de la fructosa. https://agustinasnaturales.webnode.es/_files/200000037-73304734a0/ciclacion%20cetosas.JPG
- Síntesis de maltosa, lactosa, sacarosa y celobiosa. Imágenes compuestas a partir de figuras tomadas de Lehninger y otros. (2005). Principios de Bioquímica. Omega.
- Reconocimiento de almidón con lugol. http://lh3.ggpht.com/-JKTHwf06gnQ/UQKpJFIEiUI/AAAAAAAATmc/D7nKeWq-las/Reconociendo%252520el%252520almid%2525C3%2525B3n%25255B5%25255D.jpg?imgmax=800
- Reacción del lugol con la amilosa. http://upload.wikimedia.org/wikipedia/commons/7/7f/IodineStarch_en.svg
- Cocción del almidón. Panizzolo, L. (2015). Curso: ¿Qué es cocinar para un químico? FQ.
- Natilla. https://es.m.wikipedia.org/wiki/Archivo:Custard.jpg
- Preparación de salsa a base de almidón. https://fr.wikipedia.org/wiki/Fichier:B%C3%A9chamel_in_saucepan.jpg
- Ejercicio. https://pixnio.com/es/deporte/gimnasio-y-correr/femenino-lindo-joven-aerobico-ejercicio
- Tazón con frutas y fibra. https://www.pxfuel.com/es/free-photo-ojvrj