Creación de recursos en Ciencias
Introducción: interacción materia y energía, concentración y absorbancia
3. Transmitancia versus absorbancia
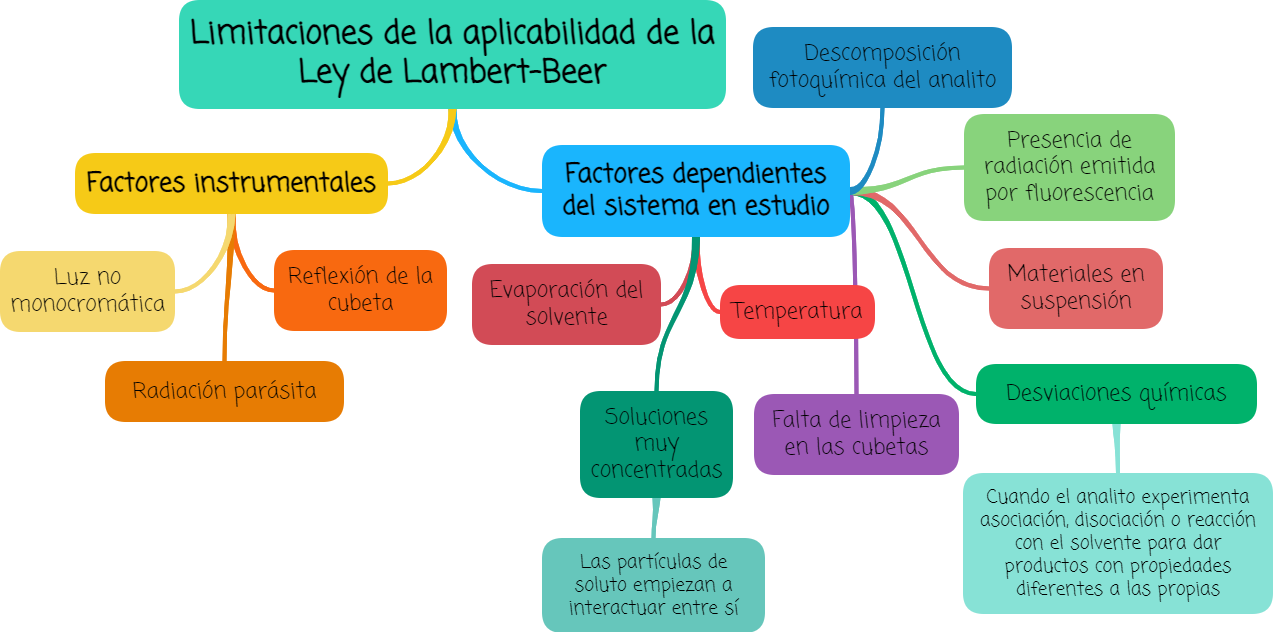
3.3. Limitaciones de la aplicabilidad de la Ley de Bouguer-Lambert-Beer
Existen diversas razones por la cual la ley de Bouguer-Lambert-Beer no se cumple, por lo tanto afectan a los resultados y la gráfica deja de ser una recta.
Algunos de estos factores pueden ser:
![]()
- Que
la luz no sea monocromática.
- Originados por radiación parásita (ejemplo luz ambiente, etc.).
- Efectos de la reflexión de la cubeta.
![]()
- Efecto de la temperatura.
- Evaporación del solvente.
- Presencia de radiación emitida por fluorescencia.
- Descomposición fotoquímica del analito.
- Falta de limpieza en las cubetas.
- Presencia de materiales en suspensión (efecto Tyndall).
- Que las soluciones sean muy concentradas, por lo que las partículas de soluto empiezan a interactuar entre sí, cambiando las propiedades eléctricas. Estas interacciones pueden alterar la capacidad absorbente de las partículas respecto a una radiación de determinada longitud de onda. Dado que el grado de interacción depende de la concentración, la existencia de este fenómeno causa desviaciones de la relación lineal entre la absorbancia y la concentración.
Como se puede observar en la siguiente gráfica la linealidad (representada con la línea de color amarillo) se mantiene a concentraciones menores a 0,01 mol/L (o 10 mmol/L) aproximadamente. Al ir aumentando la concentración de la solución, la gráfica deja de ser una recta (representada con la línea punteada de color azul).
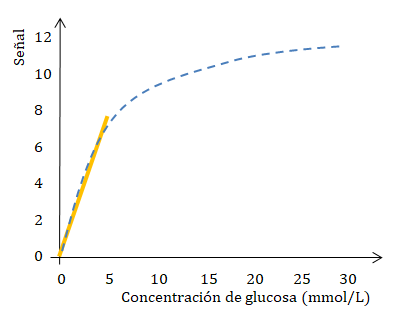
- Que hayan cambios en la naturaleza de las especies absorbentes o en las propiedades de la solución; por ejemplo ionización, disociación, etc.
Ejemplo: debidas a reacciones del absorbente con el solvente, como en el caso del dicromato en soluciones no amortiguadas.
Cr2O72- + H2O ⇄ 2 H+ + 2 CrO42-
Para cualquier longitud de onda la absortividad molar del ion dicromato y del cromato son diferentes.
![]()
En la práctica se considerará que aquellos factores no específicos como la reflexión en la superficie del recipiente o dispersión en el medio, permanecen constantes de tal forma que la disminución de la intensidad o potencia de haz de luz es debido a las partículas absorbentes localizadas en el camino óptico. Esta disminución de la intensidad de la luz depende del número y del tamaño de dichas partículas.
