Creación de recursos en Ciencias
Actividad 7: Tercer logro de Giribaldo y el proceso de la electrólisis
Observa el siguiente diagrama que representa la electrólisis de una solución de salmuera:
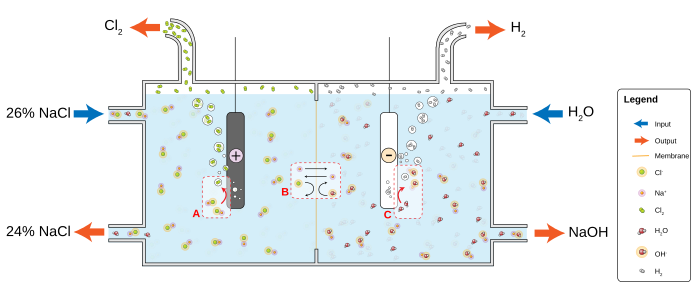
La membrana selectiva de iones (B) permite que el contraión Na+ fluya libremente, pero evita que se difundan aniones como el hidróxido (OH-) y el cloruro.
Guía de trabajo:
- ¿Qué significa el término electrólisis?
- ¿Qué diferencias existen entre la electrólisis del cloruro de sodio (NaCl) acuoso o fundido?
- ¿Cuáles son los productos de la electrólisis del cloruro de sodio en solución? Escribe las ecuaciones que lo representen.
- ¿Cuál es el proceso de oxidación que ocurre? ¿Cuál el de reducción?
- ¿Por qué se dice que el catión sodio es un ion espectador?
- ¿Cómo separó los productos de la electrólisis Giribaldo? ¿Qué diferencias presenta este procedimiento con el realizado en la celda de membrana y en la celda de mercurio?
- ¿Por qué se llama proceso de cloralkali a este proceso industrial?
- El hipoclorito de sodio en solución se prepara mediante reacción entre una solución de soda cáustica diluida y dicloro líquido o gaseoso. En vista de que la reacción libera energía (proceso exotérmico), se debe realizar acompañada por procedimientos de refrigeración. Durante todo el proceso la solución se mantiene alcalina, para disminuir la descomposición del hipoclorito de sodio, razón por la cual se emplea un exceso de soda cáustica. El pH final de la solución debe ser de 11 para mejorar su estabilidad.
Cl2 (g) + 2 NaOH(ac) → NaClO(ac) + NaCl(ac) + H2O(l)
¿Qué significa que se utilice un exceso de soda cáustica?
¿Qué masa de hipoclorito de sodio se obtendrá a partir de 10,0 L de dicloro gaseoso a una presión de 2,00 atm y una temperatura de - 20,0 °C?
¿Qué volumen mínimo de hidróxido de sodio se debe colocar para que se produzca esta reacción (recuerda que se obtiene al 32 % m/V en la electrólisis)?
¿Qué significa "para mantener la estabilidad del hipoclorito de sodio en solución su pH debe de ser 11"? ¿Qué relación guarda este hecho con el líquido Carrel propuesto por Giribaldo?
- Observa el siguiente video que muestra este proceso llevado a cabo en nuestro país (Pando, Canelones). Luego indica en qué consiste el proceso que lleva a cabo Alliance y qué diferencias presenta para con el uso de celdas de mercurio.
- ¿Qué cuidados se deben tomar al trabajar con los productos de la electrólisis del cloruro de sodio en solución, así como en el proceso posterior de obtención del hipoclorito de sodio? ¿Qué pictogramas deben llevar estos productos?
Sube todas tus respuestas en un archivo adjunto.
