Formato rejilla
Material de lectura
3. Interpretación de las transferencias de energía: entalpía
3.3. Entalpía de combustión
La variación de entalpía de combustión (ΔHcomb) representa la energía en forma de calor liberada en una combustión para 1 mol del reactivo que se quema. La combustión es un proceso exotérmico donde se libera energía.
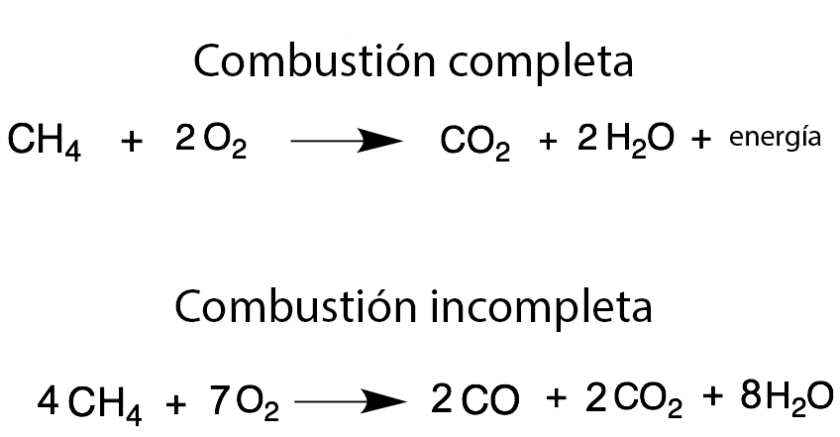
La combustión puede ser:- completa: con el aporte necesario de dioxígeno gaseoso, formándose dióxido de carbono y agua, o
- incompleta: si la cantidad de dioxígeno presente es menor a la necesaria, formándose monóxido de carbono y hollín (carbono sólido).
La siguiente tabla indica el ΔHcomb para algunas sustancias:
| Sustancia | Fórmula | ΔHcomb (kJ/mol) |
|---|---|---|
| Octano | C8H18 (l) | - 5471 |
| Glucosa | C6H12O6 (s) | - 2808 |
| Sacarosa | C12H22O11 (s) | - 5645 |
| Metano | CH4 (g) | - 802,4 |
