Química - 3º B.D.
Manos a la obra
1. Para el siguiente equilibrio representado en la figura que se encuentra a continuación:
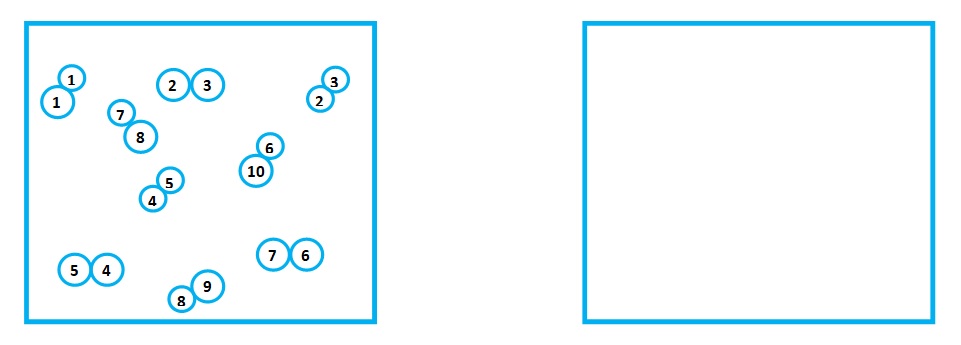
a. Escribe la ecuación química correspondiente.
b. Dibuja y enumera una situación de equilibrio después de transcurrido un
cierto tiempo a temperatura constante
( ![]() representa un átomo de hidrógeno y
representa un átomo de hidrógeno y ![]() representa un átomo de
yodo. Los átomos han sido numerados para identificarlos).
representa un átomo de
yodo. Los átomos han sido numerados para identificarlos).
2. Se ponen a reaccionar a presión y temperatura constantes 2,000 moles de dinitrógeno y 1,000 mol de dihidrógeno gaseosos ocupando un volumen de 0,41 L. Cuando el sistema alcanza el equilibrio químico hay presentes 1,6912 moles de dinitrógeno y 0,0737 moles de dihirógeno ocupando un volumen de 0,33 L.
a. Escribe una ecuación que represente el proceso.
b. Calcula las concentraciones de cada gas (expresadas en mol/L) inicialmente y cuando se alcanza el equilibrio químico.
c. ¿Qué diferencia hay entre concentración y masa? ¿Cómo lo explicas?
3. Analiza la siguiente representación gráfica y contesta:
2 SO2 (g) + O2 (g) ⇄ 2 SO3 (g)
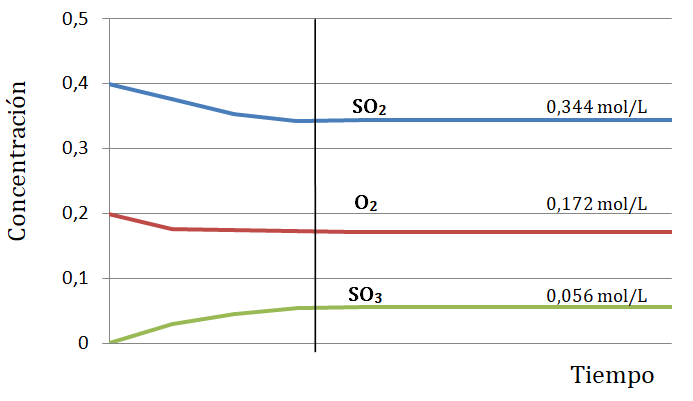
- de qué especies se parte.
- cuáles son las concentraciones iniciales.
- cuáles son las concentraciones en el equilibrio químico.
- por qué podemos afirmar que las especies se encuentran en equilibrio químico.
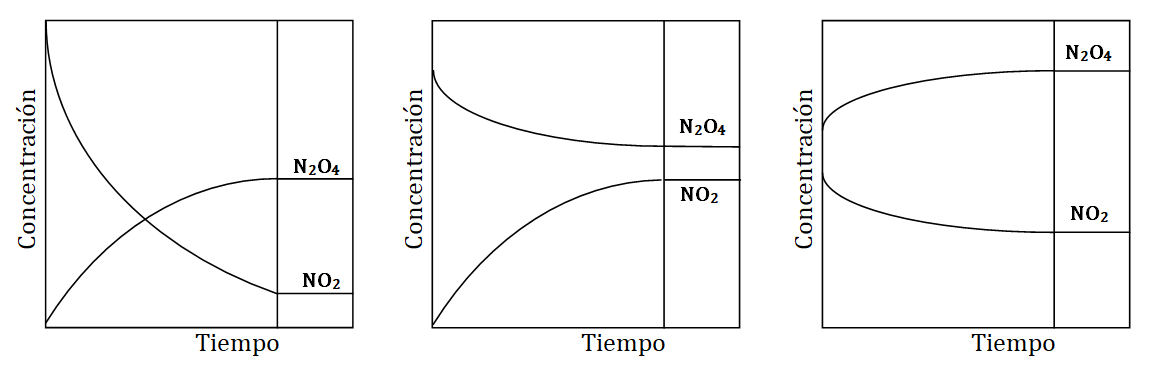
4. Elabora un análisis de las tres gráficas que se encuentran a continuación, teniendo presente sus tres niveles de información:
- Información explícita (variables y su clasificación, valores de las variables);
- Información implícita (leyendas, traducción de la información, relación entre las variables);
- Información conceptual (relaciona los conceptos trabajados en la secuencia con el contenido representado en la gráfica para interpretar y explicar la situación).
La siguiente tabla te puede ser útil para autoevaluarte.
| ¿Qué he de hacer? | Estará bien hecho si... |
|---|---|
| 1- Identificar la información explícita de la gráfica | - Sé cuál es el título de la gráfica. - Sé cuáles son las variables que se han graficado. - Clasifiqué las variables en dependiente e independiente. - Identifiqué los valores que adquieren cada una de dichas variables. |
| 2- Identificar la información implícita de la gráfica | - Interpreté las leyendas o símbolos usados, así como las unidades en las que se expresa una variable si corresponde. - Identifiqué la relación de proporcionalidad que existe entre las variables analizadas. |
| 3- Identificar la información conceptual | - Relacioné la gráfica con el contexto en el que se está trabajando. - Identifiqué qué conceptos de los trabajados en la clase se relacionan con la gráfica. |
Fuente: Adaptado de Postigo y Pozo (2000) y Sanmartí (1998, 2002 y 2018).
5. El pentacloruro de fósforo es un compuesto químico que se usa en síntesis orgánica, como agente de síntesis de polímeros, como catalizador en ciertas reacciones químicas, también en la producción de semiconductores, entre otros.
Al aumentar su temperatura, sublima para producir vapores gaseosos, y se descompone térmicamente formando dicloro gaseoso y tricloruro de fósforo gaseoso como se representa a continuación.
PCl5 (g) ⇄ PCl3 (g) + Cl2 (g)
A continuación se presenta una tabla de datos que incluye la cantidad química de estos compuestos, el volumen que ocupan y la concentración expresada en mol/L.V (L) | n PCl5 (mol) | n PCl3 (mol) | n Cl2 (mol) | V (L) | [PCl5] (mol/L) | [PCl3] (mol/L) | [Cl2] (mol/L) |
|---|---|---|---|---|---|---|---|
0,5 | 2,7816 | 0,3184 | 0,2184 | 0,5 | 5,5632 | 0,6368 | 0,4368 |
1,0 | 2,6805 | 0,4195 | 0,3195 | 1,0 | 2,6805 | 0,4195 | 0,3195 |
1,5 | 2,6052 | 0,4948 | 0,3948 | 1,5 | 1,7368 | 0,3299 | 0,2632 |
2,0 | 2,5432 | 0,5568 | 0,4568 | 2,0 | 1,2716 | 0,2784 | 0,2284 |
2,5 | 2,4899 | 0,6101 | 0,5101 | 2,5 | 0,9960 | 0,2440 | 0,2040 |
3,0 | 2,4426 | 0,6574 | 0,5574 | 3,0 | 0,8142 | 0,2191 | 0,1858 |
3,5 | 2,4000 | 0,7000 | 0,6000 | 3,5 | 0,6857 | 0,2000 | 0,1714 |
4,0 | 2,3610 | 0,7390 | 0,6390 | 4,0 | 0,5903 | 0,1847 | 0,1597 |
4,5 | 2,3250 | 0,7750 | 0,6750 | 4,5 | 0,5167 | 0,1722 | 0,1500 |
5,0 | 2,2915 | 0,8085 | 0,7085 | 5,0 | 0,4583 | 0,1617 | 0,1417 |
5,5 | 2,2601 | 0,8399 | 0,7399 | 5,5 | 0,4109 | 0,1527 | 0,1345 |
6,0 | 2,2305 | 0,8695 | 0,7695 | 6,0 | 0,3717 | 0,1449 | 0,1283 |
6,5 | 2,2025 | 0,8975 | 0,7975 | 6,5 | 0,3388 | 0,1381 | 0,1227 |
7,0 | 2,1759 | 0,9241 | 0,8241 | 7,0 | 0,3108 | 0,1320 | 0,1177 |
7,5 | 2,1506 | 0,9494 | 0.8494 | 7,5 | 0,2867 | 0,1266 | 0,1133 |
8,0 | 2,1264 | 0,9736 | 0,8736 | 8,0 | 0,2658 | 0,1217 | 0,1092 |
8,5 | 2,1032 | 0,9968 | 0,8968 | 8,5 | 0,2474 | 0,1173 | 0,1055 |
9,0 | 2,0810 | 1,0190 | 0,9190 | 9,0 | 0,2312 | 0,1132 | 0,1021 |
9,5 | 2,0596 | 1,0404 | 0,9404 | 9,5 | 0,2168 | 0,1095 | 0,0990 |
10,0 | 2,0391 | 1,0609 | 0,9609 | 10,0 | 0,2039 | 0,1061 | 0,0961 |
10,5 | 2,0192 | 1,0808 | 0,9808 | 10,5 | 0,1923 | 0,1029 | 0,0934 |
11,0 | 2,0000 | 1,1000 | 1,0000 | 11,0 | 0,1818 | 0,1000 | 0,0909 |
11,5 | 1,9814 | 1,1186 | 1,0186 | 11,5 | 0,1723 | 0,0973 | 0,0886 |
12,0 | 1,9635 | 1,1365 | 1,0365 | 12,0 | 0,1636 | 0,0947 | 0,0864 |
12,5 | 1,9460 | 1,1540 | 1,0540 | 12,5 | 0,1557 | 0,0923 | 0,0843 |
13,0 | 1,9291 | 1,1709 | 1,0709 | 13,0 | 0,1484 | 0,0901 | 0,0824 |
13,5 | 1,9127 | 1,1873 | 1,0833 | 13,5 | 0,1417 | 0,0880 | 0,0805 |
14,0 | 1,8967 | 1,2033 | 1,1033 | 14,0 | 0,1355 | 0,0860 | 0,0788 |
14,5 | 1,8811 | 1,2189 | 1,1189 | 14,5 | 0,1297 | 0,0841 | 0,0772 |
15,0 | 1,8660 | 1,2340 | 1,1340 | 15,0 | 0,1244 | 0,0823 | 0,0756 |
b. Compara ambas gráficas. ¿Qué similitudes y diferencias presentan?
