Química - 2º B.D.
Profundizando en las propiedades y estructura de los sólidos
4. Sólidos cristalinos y amorfos
![]()
Los materiales sólidos pueden pertenecer al grupo de los sólidos cristalinos o los amorfos.
En la naturaleza existen sustancias como el cloruro de sodio (NaCl), el azufre y la sacarosa (C12H22O11 - azúcar de mesa) que son sólidos en las condiciones ambientales y por lo tanto poseen las propiedades de poca compresibilidad y rigidez, además los encontramos en la naturaleza con formas geométricas características. Estas sustancias con formas características los denominamos sólidos cristalinos y los distinguimos de los no cristalinos que los denominamos amorfos.
Las propiedades de los cristales reflejan su gran ordenamiento interno. Existen en la naturaleza muchos minerales cristalinos que muestran sus caras y ángulos bien definidos como el cuarzo natural. Otras veces muchas sustancias sólidas se presentan en polvo y se puede pensar que son amorfas, pero si se examina la partícula individual bajo el microscopio, los ángulos cristalinos se pueden visualizar. Por ello debemos distinguir entre sólidos policristalinos (metales, en general) y amorfos.
El tamaño de los cristales de una sustancia puede variar dependiendo de las condiciones en que se forma el cristal.
Para distinguir claramente sólidos cristalinos de los amorfos es fundamental determinar su punto de fusión, ya que los cristalinos tienen puntos de fusión bien definidos y los amorfos no tienen puntos de fusión definidos.
Los sólidos amorfos no tienen una estructura bien definida y ordenada. Como ejemplos se incluyen la goma, algunos tipos de plásticos y el azufre amorfo.
La ruptura de un sólido cristalino produce fragmentos que tienen los mismos (o relacionados) ángulos interfaciales y las mismas características estructurales que la muestra original. Los sólidos amorfos con estructuras irregulares se rompen irregularmente para rendir piezas con aristas curvas y ángulos irregulares.
En la siguiente figura se pueden observar las diferencias en la estructura de un sólido cristalino y uno amorfo:
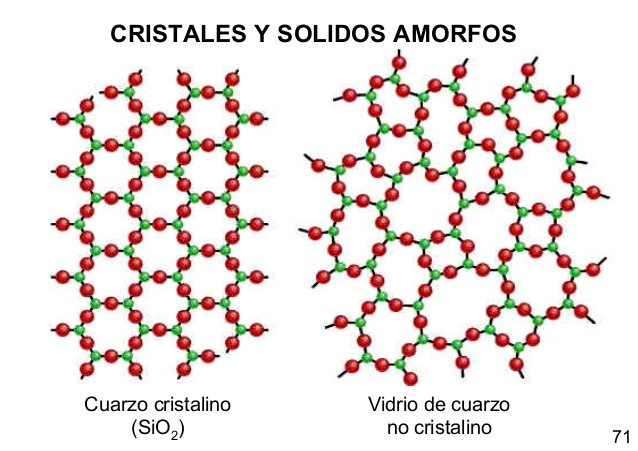
![]()
Los sistemas cristalinos dependen de la disposición simétrica y repetitiva de las caras que forman el cristal. Dicha disposición se debe al ordenamiento interno de las partículas que forman al cristal. Los cristales poseen la misma simetría que las unidades que los constituyen, porque los cristales son múltiplos repetitivos de tales celdas. Existen 7 sistemas cristalinos:
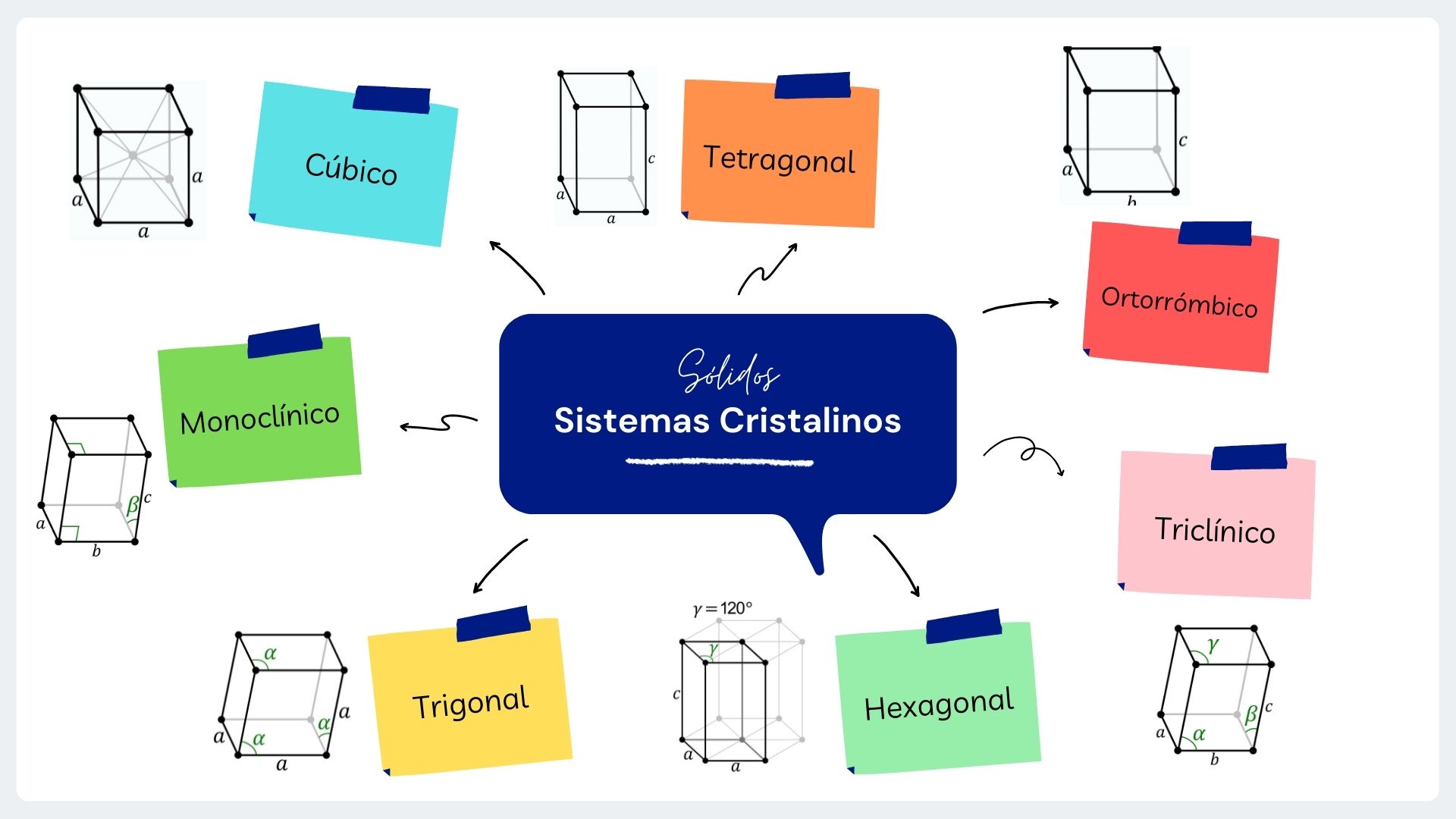
A continuación podrás observar un cuadro en el que se muestran ejemplos de los sistemas cristalinos:
| Sistema cristalino | Ejemplos | Imágenes |
|---|---|---|
| Cúbico | NaCl |  |
| Tetragonal | TiO2 (rutilo) |  |
| Ortorrómbico | KNO3 (imagen), MgSO4.7H2O |  |
| Triclínico | K2Cr2O7, CuSO4.5H2O (imagen) |  |
| Hexagonal | SiO2 (sílice) |  |
| Trigonal o romboédrico | CaCO3 (calcita) |  |
| Monoclínico | CaSO4.2H2O (caliza) |  |
